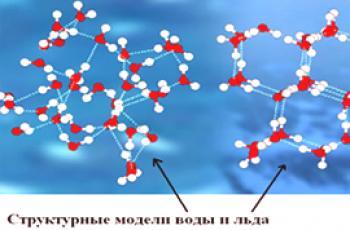
Aby bylo možné správně posoudit složení vody, je nutné studovat, co je voda v zásadě. Jak je známo z lekcí fyziky a chemie, voda je látka (kapalina) sestávající z takových chemických prvků, jako je vodík a kyslík. Voda se nachází v přírodě v několika státech, nebo spíše třech. Při nízkých teplotách krystalizuje v ledu, při vysokých teplotách se ve vodě tvoří voda a za normálních podmínek je kapalinou voda. 
Voda je součástí celého života na planetě, zejména v nás ( asi 80% ). Nemůžeme existovat bez vody v našem těle, jíst potraviny obsahující tuto tekutinu, my se vyrovnáváme za ztrátu normálního života. Nemá vůni ani chuť, ale člověk a všechny živé věci pijí vodu, protože potřebují svou životodárnou moc.
Voda pomáhá všem živým organismům růst a prospívat, v jakémkoliv agregátním stavu je to nutné a důležité. Tak, rozmrazování ledovců, dávat půdě nejužitečnější stopové prvky, protože v pevném stavu molekuly vody jsou nasyceny kyslíkem, místo toho půda dává rostlinám, a oni zase produkují kyslík, který je nezbytný pro všechny. A produkty z kuchyňské zahrady se po dešti nebo hojném zalévání vodou stávají mnohem chutnějšími.
Co se týče molekuly vody, sestává z atomů vodíku a kyslíku, které jsou umístěny velmi blízko u sebe . Zároveň se aktivně pohybují a komunikují. Není tedy žádným tajemstvím, že molekula vody je těžší než například molekula páry. V plynné molekulelátek je všechno úplně jiné. Podívejme se konkrétně na složení molekul par.

Molekuly vody
Molekuly plynné látky - páry
\ tVycházeje ze skutečnosti, že samotná voda je těžká i lehká, mění se také molekuly páry těchto vod. V každém případě však bude molekula par lehčí než molekula vody. To je způsobeno tím, že atomy pohybující se v molekule páry jsou umístěny velmi daleko a mezi sebou. Proto vzduch se zvýšenou kombinací vlhkosti při vysoké teplotě přináší více škody než užitku. Osoba nebude po dlouhou dobu schopna dýchaný vzduch dýchat. To platí pro saunu, kde je možné strávit jen několik hodin.
Pára je agregát, to znamená kapalina vázající molekulu, v tomto případě voda. Vzdálenost mezi atomy a molekulami v páru je mnohem větší než velikost samotných molekul. Atomy páry se pohybují náhodně a velmi rychle, vezmeme-li v úvahu velkou místnost, pak je pára v krátké době schopna ji naplnit. Kromě toho se pára na rozdíl od vody dokáže zmenšit. V malém prostoru je plyn schopen expandovat a vytvářet tlak, takže pokud nádobu zakryjete párou, může ji tlačit pod tlak. 
To jsou zajímavé vlastnosti páry, které lze naučit studiem teorie. V praxi je vše mnohem zajímavější, provádíme různé experimenty, na toto téma můžete udělat mnohem více objevů. A nyní srovnejme dva agregované stavy vody - kapaliny a páry. O čem jsou všichnikonkrétně se liší, co je spojuje?
Molekula vody jako taková je molekula páry, založená na jejich složení. To je běžná věc mezi nimi je tokyslík a vodík ve stejném množstvíbýt v obou molekulách. Je možné poznamenat, že se neustále a rychle odpuzují, tato vlastnost je také sjednocuje mezi sebou.
Hlavní rozdíly molekul par z molekuly vody:
- Pára se skládá z molekul, kde jsou atomy umístěny ve vzdálenosti větší, než je molekula samotná, ale ve vodě, naopak je velmi blízko. Plyny nemají žádnou formu a mohou se jak zmenšovat, tak expandovat v různých směrech, v důsledku síly, s níž se atomy a molekuly navzájem odpuzují. Voda je tekutá, na rozdíl od páry má podobu nádoby, ve které se nachází, protože molekuly jsou příliš blízko u sebe.
- Plyn může vytvářet tlak, když se molekuly vzájemně odpuzují, mohou například vytlačit korek ze šampaňského.
- A voda nemůže vyvíjet tlak na objekty, protože molekuly uvnitř vody se pohybují náhodně, spíše než kolidují přímo mezi sebou.
- Voda je chemický prvek (látka) a pára je fyzikální stav vody.
Doufáme, že jste navštívili naše webové stránky, a na vaši otázku jsme odpověděli dostatečně podrobně.