Především se budete muset vypořádat s terminologií, protože nejen mnozí považují termíny „amoniak“ a „amoniak“ za synonyma, ale zároveň označují slovo „kyselina salicylová“, protože to je taková „zkrácená verze“, která je naprosto nesprávná. Tak, amoniak je vlastní jméno jen jeden z mnoha možných sloučenin dusíku s vodíkem, ve kterém v každé molekule jsou tři atomy vodíku na atom dusíku.
Za normálních podmínek (tj. Pokojové teploty a normálního tlaku) je touto sloučeninouplyn se specifickým, velmi silným zápachem . Termín "amoniak" se běžně chápe jako slabý vodný roztok (ne více než 10%!) Hydrátu amoniaku ve vodě, zejména pro lékařské aplikace. Abnormální zkratka tohoto názvu na „plat“ je chybná - protože tato skrývá tuhou sůl vytvořenou z amoniaku a kyseliny chlorovodíkové, která má čistě lékařskou a různá domácí použití (například jako potravinářská přísada E510 nebo tavidlo při pájení výrobků ze železa) .

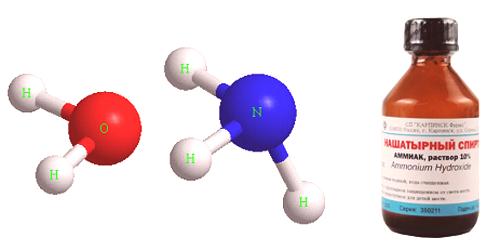
Molekula čpavku
Odkud pochází název "kapalný amoniak"?
V tomto bodě neexistuje shoda, ale současná teorie je, že alchymisté, kteří se poprvé dostali k této látce, měli vlastní myšlenku kolemchemických esencí založených na „duchech“ a „kvintesenci“. Například „duch vína“spiritus vinije víno (ethyl) alkohol, dobře známá těkavá a pachová látka, která dodává vínu určité vlastnosti.Amoniak je také velmi těkavý a páchnoucí, i když velmi zvláštní - a proto byl okamžitě zapsán do „odloučení duchů“.
Pro nespecializovaného pracovníka je obtížné sledovat, jak se za domácích podmínek může amoniak „přeměnit“ na čpavek a zpět, protože ve vzduchu kolem nás, přinejmenším ve stopových množstvích, je vždy vlhkost (voda) a čpavek, mírně řečeno. velmi lhostejný ": za pokojových podmínek může jeden objem vody rozpouštět přibližně 700 (přesně sedm set!) ekvivalentních objemů plynného amoniaku a při nule stupních toto číslo obecně vzroste na ~ 1200 objemů!
Samotné zkapalnění čpavku na lehkou mobilní tekutinu při teplotě-33 ° C , po které může být v libovolném poměru smícháno s vodou (s velkým hmotnostním podílem amoniaku, je správnější mluvit o „roztoku amoniaku ve vodě“). ", A o" roztoku vody v čpavku ").
Jaké jsou tedy mezi nimi nejdůležitější rozdíly?
Již bylo zmíněno, že amoniak je pro léčebné účely pouze slabým roztokem hydrátu amonného ve vodě. Proč je to tak důležité?
Za prvé, amoniak může být vyráběn a prodáván jako produkt ve formě koncentrovaných vodných roztoků ( z 25% a více ) - a taková řešení v každodenním životě jsou nesmírně nebezpečná! Faktem je, že koncentrované roztoky amoniaku vždy nad svým povrchem obsahují značné množství tohoto plynu, což je 1,7krát lehčí než vzduch.
Kromě toho se jeho hydrát snadno rozpadá při mírném zahřívání, které v zásadě probíháPři otevírání kontejneru s ním může způsobit uvolnění koncentrovaného "plynového polštáře" do obličeje. Proto by neměl být ani slabý kapalný amoniak podáván bez zápachu okamžitě „z láhve“, ale je nutné navlhčit vatu /ubrousek s nimi - jinak, místo toho, aby se vzrušovaly konce nervů horního dýchacího traktu (zvýšené dýchání), dojde k jeho reflexnímu zastavení!
Za druhé, koncentrované vodné roztoky amoniaku jsoužíraviny , které mohou snadno poškodit nejen lidské sliznice, ale i kůži samotnou (nemluvě o obecné otravě těla pronikáním přes ni - protože čpavek dlouhodobým kontaktem „úniky“ snadno přes kůži a přes tenkou pryž z domácnosti).
Za třetí, i jednoduché ředění koncentrovaného roztoku na „alkoholové“ podmínky s následným použitím je potenciálně spojeno snegativními důsledky , protože koncentrované roztoky jsou obvykle „technické“ a mohou obsahovat nestandardizované množství nečistot nebezpečných pro člověka. (obecně, dříve v průmyslu, taková řešení byla náhodně získána během koksování uhlí - a nakonec v procesu se uvolní masa těžkých karcinogenů!)
Za čtvrté, z čistě chemického hlediskajsou různé látky : amoniak je plyn s chemickým vzorcemNH3a amoniak je vodný roztok tohoto plynového hydrátu (ve starých učebnicích). tato sloučenina je obvykle psána ve forměNH4OH , v novější je často používánaredukci formy NH32H2O).







