Dispergované roztoky jsou systémy, ve kterých je fáze reprezentována částicemi o velikosti od 1 nm do 10 mikronů. Disperse systémy jsou obyčejné, použitý v průmyslu. Mezi ně patří: aerosoly (kapky nebo pevné částice suspendované ve vzduchu), emulze (kapky kapaliny rozpuštěné v jiné kapalině), koloidní roztoky jsou soly (dvoufázové heterogenní systémy, jejichž velikost částic je mezi emulzemi a pravými roztoky, pak Je v rozmezíod 1 do 100 nmDispergované částice mohou být v rozmanitém agregovaném stavu, soubor částic je fáze a jejich kombinace je dispergované médium (kapalné, plynné a pevné).
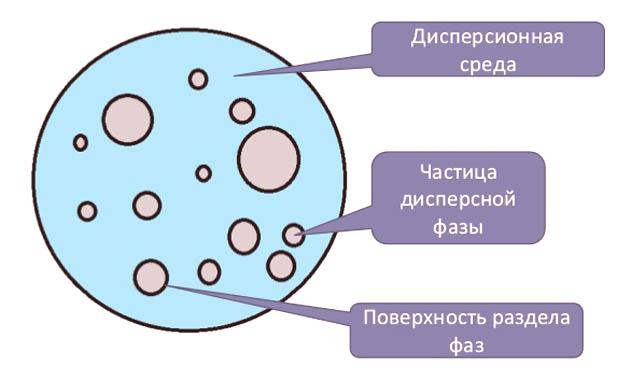
Složení disperzního systému
Vlastnosti a použití koloidních roztoků
\ tV širokém smyslu jsou v podstatě koloidyvšechny přírodní organismy a environmentální rostliny , z nichž většina odebíráme s jídlem v koloidním stavu. Na koloidy se také vztahují léčiva, některé barvy a dokonce i stavební materiály (cementové a betonové materiály, barvy a keramika, hořlavé materiály, umělá vlákna, plasty).
Kinetické vlastnosti heterogenních disperzních systémů. Pohyb je způsoben rozdílem ve velikosti částic. Tenká suspenze schopná Brownova náhodného pohybu. Například tuk přidaný do vody nebo mléko zředěné vodou. Pohyb částic koloidního roztoku je termodynamicky energeticky náročný.

OstatníKinetická vlastnost roztoků jedifúze : proces pohybu částic v důsledku rozdílů v jejich koncentracích. Tuhé hrubé částice se však neúčastní chaotického pohybu, ale hlavním důvodem jejich pohybu je oddělení hustoty fází v dispergovaném médiu. Pokud je tedy hustota větší, pak se částice postupně usazují působením gravitace - procesu sedimentace. Velmi běžný proces používaný v molekulární chemii proteinů, molekul nukleových kyselin a dokonce i bakterií. Osmotický tlak koloidů je velmi malý, protože koloid má velkou hmotnost.

Optické vlastnosti roztoku jsou způsobeny schopnostírozptylovat světlo , tj. Přítomností fenoménu opalescence (v důsledku optické nehomogenity). Je pozorováno, že když projdete světelným paprskem kyvetou, položíte před sebe čočku, pak ze strany uvidíte efekt (Tyndallův kužel). To je způsobeno závislostí velikosti částic roztoku a délkou světelného paprsku.
Disperze je pozorována, pokud je vlnová délka větší než velikost částic v p-re. Pokud mají částice stejnou velikost jako vlnová délka, paprsek jej zaokrouhluje a rozptyluje, to znamená pozoruje difrakční jev. Vzhledem ke spektru rozptylu je možné přesně určit, zda je roztok pravdivý (iontový, molekulární nebo koloidní roztok).
Opravdová řešení a jejich vlastnosti
Skutečná řešení jsou transparentní, homogenní roztoky s pevnou disperzní fází, částice menší než jeden nanometr, tedy hraniceoddělení fází v roztoku zmizí. Opravdová řešení jsou rozdělena na iontové, pokud dispergovaná fáze sestává z hydratovaných iontů (roztok chloridu sodného nebo molekulární roztok glukózy). Voda hraje nepostradatelnou součást života, protože v ní jsou rozpuštěny všechny ionty těla, díky nimž dochází ke všem metabolickým procesům. mezi buňkami.

Rozdíly mezi koloidy a skutečnými roztoky
\ tZa prvé, skutečné roztoky jsou transparentní a homogenní, částice v disperzní fázi jsou menší než nanometr. Nejsou charakterizoványdifrakcí nebo opalescencí , není tam žádný Tyndallův kužel, to znamená, že částice jsou tak malé, že nejsou ani viditelné v ultramikroskopu. Při filtraci koloidní roztoky neprocházejí papírovými filtry a skutečné filtry se snadno filtrují, což ukazuje rozdíly mezi velikostí částic dispergované fáze. Skutečné řešení prochází buněčnými membránami. Termodynamické a nestabilní, stratifikované, což je typické pro koloidní roztoky a pravdivé - nerozvrstvují.
Skutečná řešení mohou být vytvořena spontánně, bez nákladů na dodatečnou energii a koloidní roztok, to znamená, že energetická bilance pro ně není stabilní. Transformační síly mezi fází a médiem pro opravdová řešení jsou poměrně velké, takže nepotřebují stabilizátor. Mechanické vlastnosti roztoků se od sebe liší. Pravá řešení jsou odolnější, protože dispergovaná fáze je stacionární, tvoří strukturu, v níž je médium uzavřeno (například kostní tkáň).Koloidní roztok je volně dispergovaný, má tekutost, proto je koncentrace fáze a média rovnoměrně rozložena (prach, kouř nebo mlha).